 |
Tan pronto como hay daño en el ADN, como una ruptura de la doble hebra del ADN, la célula activa un mecanismo llamado respuesta al daño del ADN que actúa como una "llamada a los servicios de emergencia", explica Martínez. Las proteínas se unen rápidamente al ADN dañado para enviar señales de alarma, que serán reconocidas por otras proteínas especializadas en reparar el daño.
El objetivo de la quimioterapia es destruir las células tumorales induciendo lesiones en el ADN, que provocan el colapso y la muerte de las células cancerosas. "Al saber cómo ocurren las lesiones del ADN y cómo se reparan, aprenderemos más sobre cómo se desarrolla el cáncer y cómo podemos combatirlo. Cualquier descubrimiento nuevo en la reparación del ADN ayudará a desarrollar mejores terapias contra el cáncer, mientras protegemos nuestras células sanas", dice Martínez. .
Los investigadores han desarrollado una nueva metodología que, con la ayuda de un método de análisis de aprendizaje automático diseñado por la Unidad Confocal del CNIO, ha permitido analizar este proceso con un grado de detalle y precisión nunca antes alcanzado. "Hasta ahora, un factor limitante en el seguimiento de la cinética de reparación del ADN era la incapacidad de procesar y analizar la cantidad de datos generados a partir de imágenes tomadas por el microscopio".
Los investigadores han utilizado microscopía de alto rendimiento que permite la adquisición de miles de imágenes de células después de la inducción de daño genético. En la primera fase, introdujeron más de 300 proteínas diferentes en las células y evaluaron en un solo experimento si interferían con la reparación del ADN a lo largo del tiempo. Esta técnica ha llevado al descubrimiento de nueve nuevas proteínas que participan en la reparación del ADN.
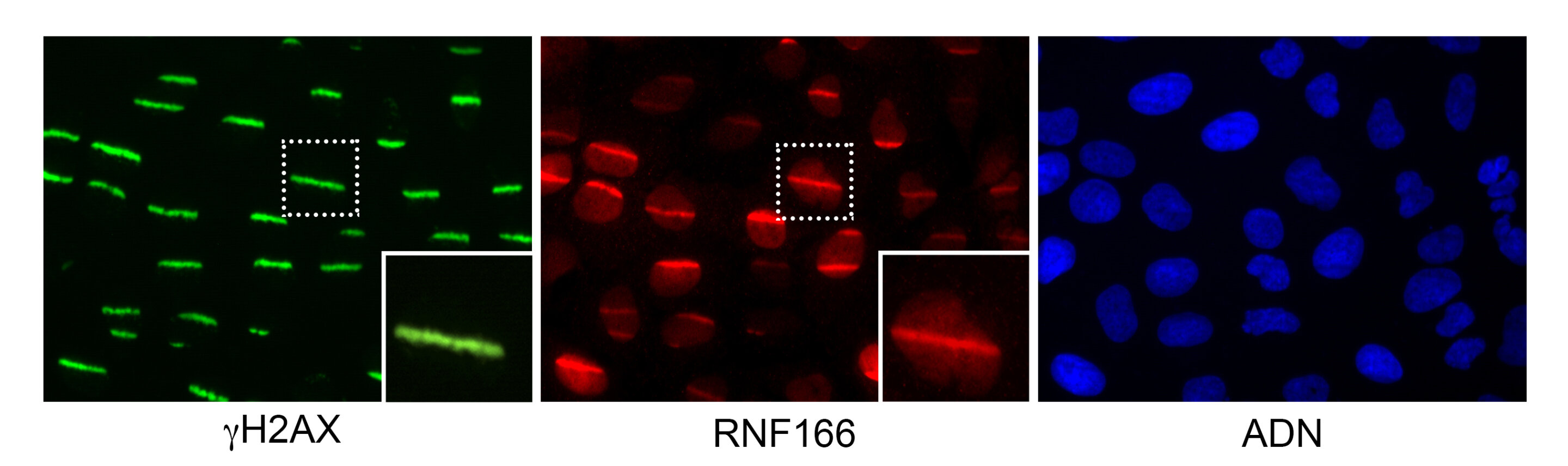
Pero los autores decidieron dar un paso más y monitorearon visualmente las 300 proteínas luego de generar daño genético. Para ello, adaptaron una técnica clásica de microirradiación de ADN, que daña el ADN con un láser UV, para ser utilizada en un formato a gran escala por primera vez y analizar el comportamiento de las 300 proteínas estudiadas.
"Vimos que muchas proteínas se adhirieron al ADN dañado, y otras hicieron todo lo contrario: se alejaron de las lesiones del ADN. El hecho de que se unieran o se eliminaran del ADN dañado para permitir el reclutamiento de proteínas reparadoras en la lesión, es una característica común de las proteínas reparadoras del ADN. Ambos fenómenos son relevantes".
Una de las proteínas descubiertas es PHF20. Los autores demostraron que esta proteína se aleja de las lesiones segundos después del daño para facilitar el reclutamiento de 53BP1, una proteína fundamental en la reparación del ADN. Las células sin PHF20 no pueden reparar su ADN correctamente y son más sensibles a la irradiación que las células normales, lo que indica que PHF20 es importante para la reparación del ADN.
Estas tecnologías ofrecen nuevas oportunidades para estudiar la reparación del ADN y manipularlo. "Una ventaja es que ambas plataformas son muy versátiles y pueden usarse para descubrir nuevos genes o compuestos químicos que afectan la reparación del ADN. Hemos evaluado cientos de proteínas en un tiempo mínimo mediante el uso de técnicas que permiten la visualización directa de la reparación del ADN".
Este trabajo ha sido financiado por el Ministerio de Ciencia e Innovación de España, el Instituto de Salud Carlos III, los Institutos Nacionales de Salud de EE. UU., El COFUND FP7 de Marie Curie, el Hospital General de Massachusetts, el Consejo de Investigación Europeo y la Investigación en Ciencias Naturales e Ingeniería. Consejo de Canadá.

0 Comentarios